科学中的是是非非
生物物理所 曾宗浩
释柘羊:虽然19世纪30年代学术界就认识到有“酶”这种能够催化有机化学反应的物质的存在。但是围绕着酶是什么的问题,却发生了一场著名的争论,这场争论的核心问题包括:1.发酵的本质是微生物活动还是化学过程?离开了微生物,酶还有没有活性?2.起催化作用的是蛋白质还是像无机催化剂那样的小分子,而蛋白质只不过是催化剂的载体?
发酵是微生物的活动,还是化学过程
薛鹦鹉:这个问题高中教科书中就有介绍了。我们现在知道,发酵是微生物活动导致的化学过程。所以,争论本不该发生。从根本上来说,这些争论与研究者对事物认知的局限性有关。况且,当时的研究者还习惯于把不同领域互相对立起来。
笨笨鸭:巴斯德(Louis Pasteur,1822-1895)根据自己的研究经验发明了巴氏消毒法:把啤酒放在摄氏五六十度的环境里,保持半小时,就可杀死啤酒里的乳酸杆菌,使啤酒不再变酸。他正确地认为发酵是微生物活动产生的现象,“是酵母把大麦酿成啤酒,……是酵母把葡萄发酵为酒”。
常翻雕:但是,凭什么他就断言酵素(酶的另一个名称)与活的细菌是不可分离的?仅凭巴氏消毒法, 只能证明细菌被杀死后,就不再存在有酶活性的物质。在啤酒内的细菌死后,原存体内的酶可能被降解、变性而失去活性。
笨笨鸭:1897年,德国化学家Eduard Buchner用将酵母细胞破碎后得到的无细胞溶液,仍然能够催化糖到酒精的化学反应,这就证明了酶是可以与细胞分离的催化剂,其活性并不需要活的细胞。
常翻雕:遗憾的是,巴斯德已经去世了。他在上帝面前一定还在喃喃自语:“李比希错了——蛋白不是必须的——使糖发酵的是酵母,是酵母的生长”。
笨笨鸭:逝者为大,你这样嘲笑一个对科学有重大贡献的人太不厚道!多伟大的人,也不可能事事正确。做了一两件正确的事就应该肯定。毕竟他发明的巴氏消毒法至今还在使用;他发明的将病原体减毒以制造疫苗的方法,挽救了多少生命。我们应该记住他的功劳,尊敬他。
薛鹦鹉:与巴斯德的观点针锋相对,德国化家李比希(Liebig, Justus von, 1803-1873)认为发酵是化学过程,糖转化为酒精这件事与酵母毫不相干,发酵必须有蛋白质存在。
常翻雕:作为著名化学家,李比希当然知道催化剂在化学反应中的重要性。但是,他凭什么就断言这催化剂就与酵母毫不相干?
笨笨鸭:智者千虑,必有一失嘛。况且他还发生过把溴元素当成氯化碘,而错失发现溴元素机会的事呐。
常翻雕:看来,这两人的共同错误,是把生物学过程和化学过程当成是互相对立、互相否定的。
笨笨鸭:在当时的知识水平和人文环境下,这是难以避免的。
具有催化活性的是蛋白质本身还是混入样品的小分子?
薛鹦鹉:由于技术条件所限,人们很难有效地纯化蛋白质样品,也很难从不纯的样品中检测出微量蛋白质,加上当时所了解的催化剂都是象金属离子那样的小分子,在对酶的化学身份的认识上出现了争论。
小贴士:由于当时没有足够灵敏的试剂来检测蛋白质的有无,著名化学家维尔施泰特(Richard Willst tter,1873-1942)因此没有能够从有酶活性的酵母提取物中探测到蛋白质。于是,他认为酶是与激素类似的、有生物活性的小分子,与酶相联系的蛋白质则被认为是真正的酶的惰性携带物。当时一些也是有影响的化学家——比如因研究糖而获得诺贝尔奖的费舍尔(Emil Fisher, 1852-1919)——同样持有这样的观点。费舍尔认为,蔗糖酶的蛋白质成分并没有表现出专一性,并且可以用化学方法同酶的催化部分分开,因此,他认为蛋白质是一种被动的、与催化作用无关的载体。
笨笨鸭:维尔施泰特和费舍尔都是著名科学家,他们认为酶是小分子与蛋白质无关的看法影响面很大。打破这种看法的进展之一是蛋白质结晶技术的完善。美国生物化学家萨姆纳(James Sumner,1887—1955)从1917年开始分离刀豆粉中的脲酶,经过多年的失败之后,最终于1926年,首先成功地制出了脲酶(脲酶能把尿素转化为二氧化碳和氨)晶体,并用化学方法证明他用结晶方法得到的纯脲酶是一种蛋白质。这是第一次得到纯化的蛋白质。1935年,美国化学家诺思洛普(J. H. Northrup,1891—1987)成功地得到了胃蛋白酶的结晶。由于脲酶和其它酶的工作,萨姆纳获得了诺贝尔化学奖。这表明,到20世纪中叶,酶是一种蛋白质的看法已获得科学界主流的承认。
常翻雕:这么说来,酶是与小分子无关的蛋白质了。如果把小分子的作用全盘否定,恐怕也有问题。
薛鹦鹉:是的。酶是蛋白质不错,但并不是与小分子无关。随着越来越多的蛋白质被认识,人们发现,在一些酶的结构中确实存在小分子和金属原子或离子。它们被称为“辅酶”。这里的“辅”字,并不表示它们一定只起辅助的作用。在一些涉及到较大能量变化的化学反应时,催化作用一定有金属原子或原子簇参与,并起关键的作用。
小贴士:光合作用分两步完成。第一步为光反应(吸收光能的反应),两个水分子被光解为一个氧分子、4个质子和4个电子;质子、电子所携带的能量最终被用来合成ATP等携能分子。第二步为暗反应(不需要光能的反应),消耗第一步所产生的携能分子所携带的能量把二氧化碳还原为糖。这里,直接利用光能分解水的任务就是由称为“释氧复合物”的一个金属氧化物原子簇完成的。
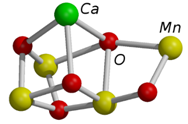
释氧复合物由一个钙(Ca+2)、4个锰和5个氧组成,其中1钙+3锰+4氧近似地分布在一个立方体的8个顶点上。水的光解就发生在这个原子簇上。基于激光脉冲实验的结果,光解过程包含5个步骤。第一步,两个水分子分别吸附在两个锰原子上。以后四步,每一步各吸收一个光子并释放一个电子和一个质子。最后一步释放一个氧分子,回到第一步。
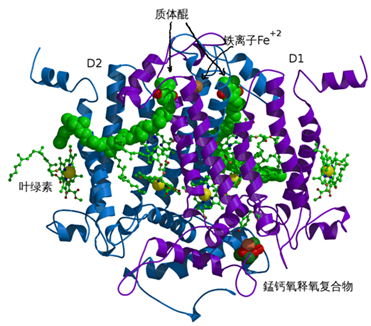
释氧复合物位于光系统II。光系统II是跨膜的蛋白复合物,含有25条以上的肽链,被众多叶绿素和无镁叶绿素所围绕。反应中心包含D1和D2两个蛋白,释氧复合物就位于D1上。图中上下取向的螺旋横跨内囊体膜,上端与膜外表面齐平,下部近似水平的螺旋紧贴膜的内表面,或在内腔中。释氧复合物释放的质子可以很方便地进入内腔,电子则需要用电子传输链送走,否则反应无法持续。
薛鹦鹉:除了释氧复合物的例子,在固氮酶中我们也可以看到铁硫原子簇。
常反雕:所以,金属原子簇总是在关键的地方起着关键的作用。
笨笨鸭:可以这么说。它们在这些地方是先锋官。但蛋白质作为一个统领,再加上其他小分子的配合,也是必不可少的。
释柘羊:回顾这段历史——蛋白质科学的历史,我们可以说,否定、否定之否定,这是科学进步的脚步。
